Устройство для интравитреального и регионарного эндолимфатического введения лекарственных препаратов и проведения блокад рефлексогенных зон в офтальмологии
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ДОПОЛНИТЕЛЬНОГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «ИНСТИТУТ ПОВЫШЕНИЯ КВАЛИФИКАЦИИ ФЕДЕРАЛЬНОГО МЕДИКО-БИОЛОГИЧЕСКОГО АГЕНТСТВА»
(ФГБОУ ДПО ИПК ФБМА России)
УСТРОЙСТВО ДЛЯ ИНТРАВИТРЕАЛЬНОГО
И РЕГИОНАРНОГО ЭНДОЛИМФАТИЧЕСКОГО
ВВЕДЕНИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ
И ПРОВЕДЕНИЯ БЛОКАД РЕФЛЕКСОГЕННЫХ ЗОН
В ОФТАЛЬМОЛОГИИ
Учебное пособие
для врачей-офтальмологов, курсантов, аспирантов,
клинических интернов и ординаторов медицинских вузов
Москва
2016
УДК: 615.032:617.747
Составители:
Заведующий кафедрой офтальмологии ФГБОУ ДПО ИПК ФБМА России д.м.н. профессор Трубилин В.Н.
Профессор кафедры офтальмологии ФГБОУ ДПО ИПК ФБМА России д.м.н. Кожухов А.А.
Доцент кафедры глазных болезней ГБОУ ВПО «Кубанского государственного медицинского университета» Министерства здравоохранения России (ГБОУ ВПО КубГМУ Минздрава России)
д.м.н. Малышев А.В.
Доцент кафедры глазных болезней ГБОУ ВПО КубГМУ Минздрава России д.м.н. Янченко С.В.
Доцент кафедры глазных болезней ГБОУ ВПО КубГМУ Минздрава России к.м.н. Лысенко О.И.
Рецензенты:
Профессор кафедры биомедицинской техники ФГБОУ ВПО «Астраханский
государственный университет» заведующая офтальмологическим отделением ЧУЗ «Медико-санитарная часть» д.м.н. Рамазанова Л.Ш.
Профессор кафедры нормальной физиологии ГБОУ ВПО КубГМУ Минздрава России д.м.н. Чередник И.Л.
«Устройство для интравитреального и регионального эндолимфатического введения лекарственных препаратов и проведения блокад рефлексогенных зон в офтальмологии»: учебное пособие. – Москва, ФГБОУ ДПО ИПК ФБМА, 2015.- 21 с.
Учебное пособие посвящено оптимизации интравитреального, регионарного эндолимфатического введения лекарственных препаратов и блокад синокаротидной рефлексогенной зоны путём применения оригинального устройства дающего возможность использования в ходе манипуляций игл калибра 30 G. Составлено в соответствии с УМК ФГОС ВПО (КубГМУ, 2014) по специальности «офтальмология» (для клинических интернов и ординаторов, врачей-курсантов) и специальности «глазные болезни» (для аспирантов вузов). Сведения, изложенные в пособии, позволяют улучшить профиль безопасности и переносимость интравитреального и эндолимфатического введения лекарственных препаратов и блокад синокаротидной рефлексогенной зоны, а также повысить субъективную готовность пациентов к прохождению повторных курсов поддерживающей терапии
Рекомендовано к изданию Ученым Советом ФГБОУ ДПО ИПК ФБМА,
протокол №___ от «___» ________ 2016 года
ПРЕДИСЛОВИЕ
Целью подготовки данного учебного пособия было информирование врачей-офтальмологов, а также лиц, проходящих последипломное обучение, о возможностях клинического применения оригинального устройства, разработанного на кафедре глазных болезней ГБОУ ВПО КубГМУ Минздрава России и тестированного на кафедре офтальмологии ФГБОУ ДПО ИПК ФБМА России (Патент на полезную модель №147763 Российская Федерация, МПК А61F9/00 // Устройство для интравитреального и регионарного эндолимфатического введения лекарственных препаратов и проведения блокад рефлексогенных зон в офтальмологии / Сахнов С.Н. (RU), Малышев А.В. (RU), Шипилов В.А. (RU), Янченко С.В. (RU) и соавт.- №147763; заявка №20144109466 от 12.03.2014; опубликовано 15 октября 2014 г.).
Указанное устройство позволяет: минимизировать степень травматизации тканей в ходе вышеперечисленных манипуляций путём применения игл калибра 30 G; повысить точность дозирования лекарственных средств; улучшить переносимость и профиль безопасности лечебных мероприятий; повысить субъективную готовность пациентов к прохождению повторных курсов терапии.
В настоящем издании приводятся данные о преимуществах клинического применения разработанного устройства, сравнительно с известными подходами, включающими использование игл калибра 27 G.
Учебное пособие может быть рекомендовано для обучения врачей-курсантов, проходящих повышение квалификации по специальности «офтальмология», клинических интернов и ординаторов, аспирантов вузов.
ВВЕДЕНИЕ
С целью достижения максимального терапевтического эффекта в офтальмологии используют интравитреальное и региональное эндолимфатическое введение лекарственных препаратов, а также такой способ лечебного воздействия как блокада синокаротидной рефлексогенной зоны (Бойко Э.В. и соавт., 2010; Егоров Е.А. и соавт., 2011; Ерёменко А.И. и соавт., 2006, 2010; Максимов И.Б. и соавт., 2007; Янченко С.В. и соавт., 2008; Aiello L.P. et al., 2004; Peyman G.A., 2009).
Известным медицинским инструментом для введения лекарственных веществ вышеуказанными путями является шприц с инъекционной иглой. При этом большое значение имеют характеристики инъекционной иглы. От них зависит легкость пенетрации тканей (пенетрирующее усилие или усилие прокола), точность попадания в определенные анатомические структуры, стабильность положения иглы в тканях, степень травматизации тканей, а, следовательно, и болезненность инъекции.
Одной из основных характеристик инъекционной иглы является ее калибр (G). Этот параметр определяет величину просвета внутренней части иглы, по которой протекает раствор. Чем больше число G, тем меньше просвет, и, следовательно, тем меньше внутренний и наружный диаметр иглы. До настоящего времени в офтальмологии при проведении вышеуказанных процедур в основном используют иглы калибра 27 G. Однако их применение сопряжено со следующими недостатками:
- достаточно большой внутренний диаметр иглы и её канюли приводит к депонированию препаратов и нарушению их задаваемого дозирования;
- при выполнении интравитреальных инъекций сохраняется высокий уровень дискомфорта и имеется риск возникновения потенциально опасного осложнения – вставления волокон стекловидного тела в склеростому, требующего наложения шва;
- недостаточно хорошая переносимость регионарного эндолимфатического введения лекарственных препаратов и блокад синокаротидной рефлексогенной зоны (дискомфорт во время и после манипуляции) и риск возникновения осложнений, влекущие за собой отказ пациентов от прохождения полного курса лечения и проведения повторных курсов терапии.
Указанные обстоятельства определяют актуальность дальнейшей оптимизации способов интравитреального (ИВ) и регионального эндолимфатического введения лекарственных препаратов (ЭВ), а также блокад синокаротидной рефлексогенной зоны (БСЗ).
В связи с этим на кафедре глазных болезней ГБОУ ВПО КубГМУ было разработано оригинальное устройство (Патент на полезную модель №147763 Российская Федерация; заявка №20144109466 от 12.03.2014; опубликовано 15 октября 2014 г.), позволяющее использовать в ходе ИВ, ЭВ и БСЗ карпульные иглы калибра 30 G и, соответственно, минимизировать травматизацию тканей в ходе лечебного воздействия.
Далее в пособии будет рассмотрены: сущность разработанного устройства, результаты его доклинического тестирования, а также итоги применения устройства в клинических условиях, в том числе, сравнительно с существующими лечебными подходами.
УСТРОЙСТВО ДЛЯ ИНТРАВИТРЕАЛЬНОГО И РЕГИОНАРНОГО ЭНДОЛИМФАТИЧЕСКОГО ВВЕДЕНИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ И ПРОВЕДЕНИЯ БЛОКАД РЕФЛЕКСОГЕННЫХ ЗОН
Разработанное устройство для интравитреального и регионального эндолимфатического введения лекарственных препаратов, а также блокад синокаротидной рефлексогенной зоны включает шприц, иглу калибра 30 G и оригинальный трёхступенчатый полый переходник, позволяющий соединять шприц и иглу (рисунок 1). Игла имеет канюлю для присоединения её к переходнику. Канюля иглы и вторая ступень переходника имеют соосно-расположенную на соответствующих поверхностях резьбу, а внутренняя полость первой ступени переходника выполнена с конусностью для соединения с наконечником шприца. Для повышения надёжности фиксации иглы третья ступень переходника выполнена в виде усечённого конуса, плотно входящего в коническую часть канюли иглы.
Перед использованием устройство необходимо собрать (рисунок 1): для этого первая ступень переходника (4) плотно соединяется с наконечником шприца (2). Затем во внутреннюю полость переходника вставляется проксимальный конец карпульной иглы 30 G (12), при этом цилиндрическая часть канюли карпульной иглы (8) навинчивается на поверхность с резьбой (11) второй ступени переходника (5), а третья ступень переходника (6) плотно вставляется во внутреннюю полость конусной части канюли карпульной иглы (9). Сборка устройства не вызывает каких либо затруднений, её этапы представлены на рисунке 2.
Техническим результатом использования устройства является обеспечение оптимальных условий для проведения интравитреального, эндолимфатического введения препаратов и блокад синокаротидной зоны путём минимизации потерь лекарственного средства и повышения точности его дозирования, улучшения переносимости и профиля безопасности лечебного воздействия, а также повышения готовности пациентов к прохождению повторных курсов терапии.
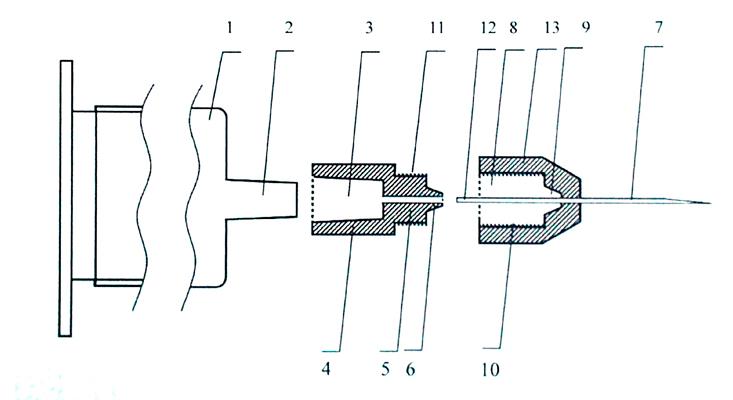
Рисунок 1. Устройство для интравитреального и эндолимфатического введения лекарственных препаратов и проведения блокад синокаротидной зоны:
1-корпус шприца; 2-наконечник шприца; 3-разработанный переходник (нержавеющая сталь марки 12Х18Н10Т или полипропилен); 4-первая ступень переходника; 5-вторая ступень переходника; 6-третья ступень переходника; 7-карпульная игла калибра 30 G; 8-цилиндрическая часть канюли карпульной иглы; 9-конусная часть канюли карпульной иглы; 10-резьба на внутренней поверхности цилиндрической части канюли карпульной иглы; 11-резьба на наружной поверхности второй ступени переходника; 12-проксимальный конец карпульной иглы; 13-канюля карпульной иглы
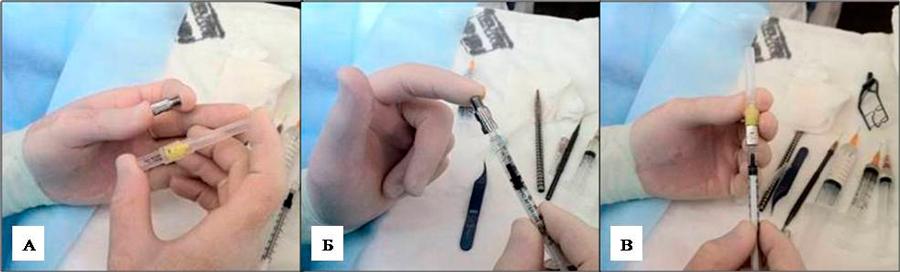
Рисунок 2. Сборка устройства для интравитреального и эндолимфатического введения лекарственных препаратов и проведения блокад синокаротидной зоны:
А – разработанный переходник и карпульная игла 30 G; Б – соединение переходника и шприца; В – соединение переходника и иглы 30 G
РЕЗУЛЬТАТЫ ДОКЛИНИЧЕСКОГО ТЕСТИРОВАНИЯ РАЗРАБОТАННОГО УСТРОЙСТВА
Доклиническая апробация устройства включала его оценку сравнительно с известным инструментом для интравитреального и эндолимфатического введения лекарственных препаратов и проведения блокад синокаротидной зоны (шприц с иглой 27 G). Для этого производили забор 500 мкл 0,9% физиологического раствора в разработанное устройство и известный инструмент. Затем жидкость вводили в пробирку Эппендорфа объёмом 1000 мкл и производили измерение её объёма при помощи автоматической пипетки для забора биологических жидкостей. Объём депонированной жидкости в разработанном устройстве (основная группа) и известном инструменте (контроль) определяли по разности между её исходным объёмом (500 мкл) и объёмом в пробирке Эппендорфа. В каждой группе производили по 50 измерений, рассчитывали среднее (М) и его стандартное отклонение (s). Достоверность различий оценивали по методу Стьюдента.
Доклиническое тестирование устройства показало, что остаточный объём (депонирование) лекарственного препарата при его применении составляет 20,1±2,1 мкл, что достоверно меньше (p<0,05), чем при использовании шприца и иглы 27 G (39,8±3,5 мкл).
Как следует из представленных данных (таблица 1), применение предлагаемого устройства позволяет минимизировать потери лекарственного средства в ходе манипуляции за счёт снижения объёма депонирования препарата. В свою очередь это позволяет: повысить точность дозированного введения лекарственных средств (что особенно важно при интравитреальном введении); минимизировать необоснованное использование дорогостоящих препаратов (например, ранибезумаба).
Таблица 1. Сравнительный анализ использования предлагаемого устройства и известного инструмента
|
№ |
анализируемый показатель (М±s)
|
шприц и игла 27G |
шприц, переходник и игла 30G |
выводы |
|
1 |
остаточный объём (депонирование) лекарственного вещества, мкл |
39,8±3,5 |
20,1±2,1* |
применение предлагаемого устройства позволяет сделать более точным дозированное введение лекарственного препарата за счёт минимизации его потерь в результате депонирования в используемом устройстве |
|
Примечание: M – среднее по группе; s – стандартное квадратическое отклонение; достоверность различий показателей между группами: * р < 0,05 |
||||
РЕЗУЛЬТАТЫ КЛИНИЧЕСКОГО ТЕСТИРОВАНИЯ РАЗРАБОТАННОГО УСТРОЙСТВА
Тестирование устройства проводилось на клинической базе кафедры глазных болезней ГБОУ ВПО КубГМУ Минздрава России - в офтальмологическом отделении Государственного Бюджетного Учреждения Здравоохранения «Научно-Исследовательский Институт – Краевая клиническая больница №1 им. проф. С.В. Очаповского Министерства Здравоохранения Краснодарского края (ГБУЗ «НИИ-ККБ№1), а также на кафедре офтальмологии ФГБОУ ДПО ИПК ФБМА России. Исследование выполнялось с разрешения локальных этических комитетов, у всех пациентов получали информированное согласие.
Было проведено обследование 150 больных 2-го периода зрелого и пожилого возраста (по классификации ВОЗ). Пациенты с офтальмологическими заболеваниями, требующими лечения с применением интравитреального или эндолимфатического введения лекарственных препаратов или проведения блокад синокаротидной зоны, были разделены на 3 группы по 50 пациентов. В пределах каждой группы были выделены основная и контрольная подгруппы (по 25 человек). Больные основной группы получали манипуляции (ИВ или ЭВ или БСЗ) с использованием предлагаемого устройства (шприц, переходник, игла 30 G). Пациентам контрольных подгрупп аналогичные лечебные мероприятия осуществляли с применением известного медицинского инструмента (шприц, игла 27 G).
Критериями эффективности применения предлагаемого устройства были переносимость и безопасность его использования: дискомфорт во время манипуляции и/или болезненность после неё (в баллах 3-балльной шкалы, где 0-отсутствие симптома, 1-лёгкие проявления, 2-умеренные проявления, 3-выраженные проявления симптома); частота возникновения осложнений (%); готовность пациентов к осуществлению полного курса инъекций и/или прохождению повторных курсов поддерживающего лечения (%).
Для интравитреального введения использовали рекомбинантную проурокиназу /«Гемаза»/ (Бойко Э.В. и соавт., 2010). Содержимое ампулы (5000 МЕ) растворяли в 1,0 мл 0,9% физраствора, затем 100 мкл полученной смеси дополнительно разводили 100 мкл физраствора. Интравитреально вводили 50-60 мкл полученного раствора однократно.
Эндолимфатическое введение лекарственных препаратов (0,5 мл 2% лидокаина и 0,5 мл пентоксифиллина) проводили подкожно на глубину 1,0 см в точку, расположенную на 1,0 см ниже и медиальнее вершины сосцевидного отростка /1 раз в сутки, с обеих сторон, №8 на курс/ (Ерёменко А.И. и соавт., 2006; 2010).
Блокады синокаротидной зоны проводили по модифицированной методике, принятой на кафедре глазных болезней КубГМУ. При этом 4,0 мл 2% лидокаина или 1% рихлокаина вводили подкожно на глубину 0,5-1,0 см в проекции синокаротидной рефлексогенной зоны, предпосылая ходу иглы струю анестетика /через день, на каждой стороне, по №5 на курс/ (Ерёменко А.И. и соавт., 2006; Янченко С.В., Ерёменко А.И., Шипилов В.А. и соавт., 2008).
Фармакологическое сопровождение интравитреальных инъекций включало: инстилляции фторхинолона четвёртого поколения - 0,5% моксифлоксацина («Вигамокс») и высокоактивного нестероидного противовоспалительного препарата – 0,1% непафенака («Неванак») за три дня до манипуляции, в день её проведения и в течение 5 дней после ИВ /5 раз в сутки/ (Wagner R.S. et al., 2005). Для профилактики транзиторной офтальмогипертензии в день ИВ использовали инстилляции комбинированного средства, включающего ингибитор карбоангидразы и 0,5% тимолол («Азарга»).
Статистическая обработка включала: расчёт среднего по выборке (М) и его стандартного отклонения (s); методы описательной статистики (расчёт частоты осложнений и/или побочных эффектов, %). Достоверность различий оценивали при помощи критерия Стьюдента и χ2.
Клиническая апробация предлагаемого устройства показала, что уровень дискомфорта при выполнении с его помощью интравитреального введения рекомбинантной проурокиназы составил 0,3±0,01 баллов, в то время как при использовании шприца и иглы 27 G – 1,48±0,09 баллов. Различие было достоверным (р<0,05). При использовании предлагаемого устройства во всех случаях проводилась прямая склеростомия, однако вставления стекловидного тела в склеростому не отмечалось. При проведении ИВ с помощью шприца и иглы 27 G формировали тоннельную склеростому, однако в 2 случаях (8%) отмечалась её неполная адаптация, что потребовало наложения шва. Субконъюнктивальные кровоизлияние после ИВ при использовании шприца и иглы 27 G отмечалось в 24%, а при использовании разработанного устройства – в 8%. Указанные различия были достоверными (χ2 > 3).
Необходимо отметить, что на фоне фармакологического сопровождения (инстилляции препаратов «Вигамокс», «Неванак», «Азарга») ни у одного из 50 пациентов не отмечалось инфекционных и/или воспалительных осложнений, а также транзиторной офтальмогипертензии.
При регионарном эндолимфатическом введении смеси лекарственных препаратов с использованием предлагаемого устройства дискомфорт во время манипуляции достигал 0,5±0,02 баллов, а болезненность в месте инъекции после манипуляции составила 0,2±0,01 баллов. Указанные показатели были достоверно меньше, чем при ЭВ, проводившемся с применением шприца и иглы 27 G (соответственно, 1,4±0,1 и 1,3±0,07 баллов; р<0,05). Подкожные кровоизлияния в месте инъекции при использовании известного инструмента отмечались в 24%, а при использовании предлагаемого устройства – в 5% (χ2 > 3). В группе пациентов, получавших ЭВ с применением разработанного устройства ни один пациент не отказался от прохождения полного курса терапии, а готовность к проведению повторных курсов составила 96%. При использовании для ЭВ шприца и иглы 27 G 12% пациентов отказались от прохождения полного курса лечения в связи с субъективным дискомфортом после манипуляции, а готовность к повторным курсам терапии составила 76%. Данные различия были достоверными (χ2 > 3).
Субъективный дискомфорт при выполнении блокад синокаротидной рефлексогенной зоны с применением предлагаемого устройства составил – 0,6±0,02 баллов, болезненность в месте инъекции после манипуляции – 0,28±0,01 баллов. Аналогичные показатели при использовании известного инструмента были достоверно выше (соответственно, 1,7±0,18 баллов и 1,35±0,11 баллов; р<0,05). Среди пациентов, получавших БСЗ с использованием иглы 27 G, 16% наблюдавшихся отказались от полного прохождения курса терапии, о готовности к повторным курсам поддерживающего лечения заявили 72%. Вместе с тем в группе больных, которым проводились БСЗ с применением предлагаемого устройства лишь один пациент (4%) отказался от полного курса лечения, а к проведению повторных курсов терапии были готовы 96% больных.
КЛИНИЧЕСКИЕ ПРИМЕРЫ ПРИМЕНЕНИЯ РАЗРАБОТАННОГО УСТРОЙСТВА, СРАВНИТЕЛЬНО С ТРАДИЦИОННЫМИ ПОДХОДАМИ
Клинический пример №1
Пациент Р., 52 лет. Диагноз: гемофтальм левого глаза.
Пациенту назначена гемостатическая и рассасывающая терапия, включающая однократное интравитреальное введение препарата «Гемаза». В условиях операционной после парацентеза роговицы на 3 ч.м. (для исключения повышения уровня внутриглазного давления в послеоперационном периоде) через плоскую часть цилиарного тела в полость стекловидного тела с помощью предлагаемого устройства, введена гемаза в стандартном разведении в объеме 50 мкл. Для этого первую ступень переходника плотно соединили с наконечником шприца, во внутреннюю полость переходника вставили проксимальный конец карпульной иглы 30 G, цилиндрическую часть канюли карпульной иглы навинчивали на поверхность с резьбой второй ступени переходника, а дистальную ступень переходника плотно вставляли во внутреннюю полость конусной части канюли карпульной иглы. После этого провели забор и интравитреальное введение лекарственного препарата. Вставления стекловидного тела в склеростому не наблюдалось. В зоне инъекции кровоизлияния под конъюнктиву не произошло. Субъективный дискомфорт во время манипуляции составил 1 балл.
Клинический пример №2
Пациент К., 57 лет. Диагноз: гемофтальм правого глаза.
Пациенту назначена гемостатическая и рассасывающая терапия, включающая однократное интравитреальное введение препарата «Гемаза». В условиях операционной после парацентеза роговицы на 3 ч.м. (для исключения повышения уровня внутриглазного давления в послеоперационном периоде) через плоскую часть цилиарного тела в полость стекловидного тела с помощью шприца с иглой, имеющей калибр 27G, введена гемаза в стандартном разведении в объеме 50 мкл. В склеростому вставилось стекловидное тело, что потребовало дополнительной герметизации доступа (наложения швов). В зоне инъекции образовалось локальное кровоизлияние под конъюнктиву. Субъективный дискомфорт во время манипуляции составил 2 балла.
Клинический пример №3
Пациент О., 59 лет. Диагноз: хроническая сосудистая оптическая нейропатия левого глаза.
Пациенту назначен курс лечения: сосудорасширяющая и метаболическая терапия, включающая эндолимфатическое введение пентоксифиллина с лидокаином. В условиях процедурного кабинета выполнено эндолимфатическое (подкожно, в точке, расположенной на 1,0 см ниже, и 1,0 см медиальнее вершины сосцевидного отростка) введение 40 мг (2 мл) пентоксифиллина + 1 мл 2% лидокаина болюсно с использованием предлагаемого устройства.
Субъективный дискомфорт во время манипуляции составил 1 балл. Болезненность в месте инъекции после манипуляции составила 0 баллов. Кровоизлияний в месте инъекций не наблюдалось. Пациент прошел полный курс ЭВ и подтвердил готовность к проведению повторных курсов регионарного эндолимфатического введения лекарственных препаратов.
Клинический пример №4
Пациент Б., 58 лет. Диагноз: хроническая сосудистая оптическая нейропатия левого глаза.
Пациенту назначен курс лечения: сосудорасширяющая и метаболическая терапия, включающая эндолимфатическое введение пентоксифиллина с лидокаином. В условиях процедурного кабинета выполнено эндолимфатическое (подкожно, в точке, расположенной на 1,0 см ниже, и 1,0 см медиальнее вершины сосцевидного отростка) введение 40 мг (2 мл) пентоксифиллина + 1 мл 2% лидокаина болюсно с помощью шприца с иглой, имеющей калибр 27G.
Субъективный дискомфорт во время манипуляции составил 3 балла. Болезненность в месте инъекции после манипуляции составила 2 балла. После 7 процедуры в месте инъекций появилось кровоизлияние, пациент отказался от прохождения полного курса ЭВ и проведения повторных курсов лечения.
Клинический пример №5
Пациент П., 56 лет. Предварительный диагноз: острая сосудистая оптическая нейропатия в виде сосудистого ретробульбарного неврита правого глаза.
С диагностической, а после подтверждения диагноза – с лечебной целью на стороне пораженного глаза проведена блокада синокаротидной зоны бензофурокаином. В условиях процедурного кабинета выполнена блокада синокаротидной зоны (после анестезии кожи 1% раствором бензофурокаина у внутреннего края грудиноключично-сосцевидной мышцы на уровне подъязычной кости, подкожно вводят 3-4 мл 1% раствора бензофурокаина) с помощью предлагаемого устройства.
Субъективный дискомфорт во время манипуляции составил 1 балл. Болезненность в месте инъекции после манипуляции составила 1 балл. Кровоизлияний в месте инъекций не наблюдалось, пациент получил полный курс лечения и подтвердил готовность к проведению повторных курсов СКБ.
Клинический пример №6
Пациент Н., 55 лет. Предварительный диагноз: острая сосудистая оптическая нейропатия в виде ишемического отека ДЗН левого глаза.
С диагностической, а после подтверждения диагноза – с лечебной целью на стороне пораженного глаза проведена блокада синокаротидной зоны бензофурокаином. В условиях процедурного кабинета выполнена блокада синокаротидной зоны (3-4 мл 1% раствора бензофурокаина с помощью шприца с иглой, имеющей калибр 27G).
Субъективный дискомфорт во время манипуляции составил 3 балла. Болезненность в месте инъекции после манипуляции составила 2 балла. После 6 процедуры в месте инъекций появилось кровоизлияние, но пациент продолжил лечение и подтвердил готовность к проведению повторных курсов СКБ.
ЗАКЛЮЧЕНИЕ
Таким образом, использование предлагаемого устройства, включающего оригинальный переходник, соединяющий шприц и иглу 30 G, позволяет обеспечить оптимальные условия для проведения интравитреального, эндолимфатического введения препаратов и блокад синокаротидной зоны.
Предлагаемое устройство позволяет:
- минимизировать потерю лекарственного вещества в ходе манипуляции, что даёт возможность более точно дозировать его введение и исключить необоснованный расход;
- улучшить профиль безопасности интравитреального и эндолимфатического введения лекарственных препаратов и блокад синокаротидной рефлексогенной зоны путём минимизации риска возникновения осложнений;
- улучшить переносимость интравитреального и эндолимфатического введения лекарственных препаратов и блокад синокаротидной рефлексогенной зоны;
- повысить субъективную готовность пациентов к прохождению повторных курсов поддерживающего лечения.
Приведенные факты позволяют прийти к заключению, что предлагаемое устройство может быть рекомендовано к широкому использованию в офтальмологической практике.
ЛИТЕРАТУРА
- Бойко Э.В., Сосновский С.В., Березин Р.Д. и соавт. Интравитреальные инъекции: теория и практика // Офтальмологические ведомости. 2010. Т. III, №2. С. 28-35.
- Егоров Е.А., Алексеев В.Н., Астахов Ю.С. и соавт. Рациональная фармакотерапия в офтальмологии. Руководство для врачей, 2-е издание. Москва: «Литтерра», 2011. 1059 с.
- Ерёменко А.И., Каленич Л.А., Янченко С.В. Клиническая эффективность способов эндолимфатического регионарного введения, внутрикаротидной инфузии лекарственных препаратов и блокад синокаротидной зоны в лечении ишемических оптических нейропатий // Офтальмологический журнал. 2006. №3. С. 151-153.
- Ерёменко А.И., Янченко С.В. Оптимизация терапии возрастной формы синдрома «сухого глаза // Офтальмологические ведомости. 2010. Т. III, №2. С. 73-80.
- 5. Максимов И.Б., Нероев В.В. Ретиналамин. Нейропротекция в офтальмологии. СПб.: Наука, 2007. 160 с.
- 6. Сахнов С.Н., Малышев А.В., Шипилов В.А., Янченко С.В., Гаспарян К.К., Сухинин А.А. Пат. на полезную модель №147763 Российская Федерация, МПК А61F9/00. Устройство для интравитреального и регионарного эндолимфатического введения лекарственных препаратов и проведения блокад рефлексогенных зон в офтальмологии / ГБОУ ВПО КубГМУ Минздрава России (RU), Сахнов С.Н. (RU), Малышев А.В. (RU), Шипилов В.А. (RU), Янченко С.В. (RU), Гаспарян К.К. (RU), Сухинин А.А. (RU).- №147763; заявка №20144109466 от 12.03.2014; опубликовано 15 октября 2014 г.
- 7. Янченко С.В., Ерёменко А.И., Шипилов В.А. и соавт. Блокады синокаротидной рефлексогенной зоны в комплексной терапии вторичного комбинированного гипосекреторного синдрома «сухого глаза» // Вестник новых медицинских технологий. 2008. Том XV, №3. С. 197-199.
- 8. Янченко С.В., Шипилов В.А., Сахнов С.Н., Малышев А.В, Гаспарян К.К., Сухинин А.А., Карапетов Г.Ю. Устройство для интравитреального и регионарного эндолимфатического введения лекарственных препаратов и проведения блокад рефлексогенных зон в офтальмологии // Офтальмология. 2014. Т. 11, №3. С. 56-62.
- Aiello L.P., Brocker A.J., Chang S. et al. Evolving guidelines for intravitreal injections // Retina. 2004. Vol. 24. P. 3-19.
- Peyman G.A., Lad E.M., Moshfeghi D.M. Intravitreal injection of therapeutic agents // Retina. 2009. Vol. 29. P. 181-189.
- Wagner R.S., Abelson M. et al. Evaluation of moxifloxacin, gatifloxacin, ofloxacin and levofloxacin concentrations in human conjunctival tissue // Arch. Ophthal. 2005. Vol. 123. P. 1282-1283.
СОДЕРЖАНИЕ
|
|
Страница |
|
3 |
|
4 |
|
6 |
|
8 |
|
10 |
|
14 |
|
18 |
|
19 |
Назад в «Готовятся к публикации»
